Dott. Antonio Daffinà
proctologoaroma.it
La Sindrome dell'Intestino Irritabile: una guida aggiornata per i pazienti
A cura del Dott. A. Daffinà, chirurgo coloproctologo. Revisione del testo aprile 2026
Quello che devi sapere subito
La Sindrome dell'Intestino Irritabile (SII), conosciuta anche come IBS (Irritable Bowel Syndrome), è un disturbo cronico dell'intestino che colpisce circa il 5-10% della popolazione mondiale, con una prevalenza leggermente maggiore nelle donne e nei soggetti al di sotto dei 50 anni.
Un tempo veniva chiamata colite spastica o colon irritabile, termini ormai superati. Oggi la comunità scientifica internazionale la classifica tra i disturbi dell'interazione cervello-intestino (disorders of gut-brain interaction), una definizione che riflette molto meglio ciò che sappiamo sulla sua natura: non si tratta di un problema solo dell'intestino, né solo della mente, ma di un'alterazione della comunicazione tra i due.
Punti chiave:
-
La SII non è una malattia immaginaria e non è "solo stress". È una condizione riconosciuta dalla comunità scientifica internazionale, con meccanismi biologici documentati che coinvolgono l'intestino, il sistema nervoso e il microbiota
-
Non è pericolosa per la vita, ma può essere molto invalidante: uno studio ha riportato che la maggioranza dei pazienti accetterebbe di rinunciare a 10-15 anni di aspettativa di vita pur di guarire istantaneamente
-
È una condizione trattabile: la maggior parte dei pazienti migliora significativamente con un approccio combinato che include modifiche alimentari, gestione dello stress e, quando necessario, farmaci mirati
-
La SII può avere un impatto considerevole su molte condizioni coloproctologiche (emorroidi, ragadi, prolassi, incontinenza), peggiorandone l'evoluzione, ritardandone la guarigione o favorendo le recidive. Questo aspetto viene spesso sottovalutato
-
Il trattamento richiede tempo, costanza e un rapporto di fiducia con il proprio medico. Non esistono soluzioni rapide, nonostante ciò che si legge sui social media o nelle pubblicità di integratori
Le informazioni contenute in questa pagina hanno finalità esclusivamente informativa e non sostituiscono in alcun modo la visita medica specialistica. In caso di sintomi, rivolgiti al tuo medico di base o a uno specialista.
In questa pagina
Usa i link qui sotto per navigare direttamente alla sezione che ti interessa, oppure prosegui nella lettura.
Cos'è davvero la Sindrome dell'Intestino Irritabile
Per molto tempo la SII è stata considerata un disturbo "funzionale", un termine che nella pratica clinica veniva spesso interpretato — erroneamente — come "non c'è niente di reale". Questa interpretazione ha causato sofferenza e frustrazione in milioni di pazienti che si sentivano dire che il loro problema era "tutto nella testa".
La realtà è molto diversa. La ricerca degli ultimi vent'anni ha dimostrato che nella SII esistono alterazioni biologiche documentabili: modifiche nella sensibilità dei nervi intestinali, alterazioni della motilità, attivazione del sistema immunitario della mucosa, squilibri del microbiota e anomalie nella comunicazione tra cervello e intestino. Non si tratta di un singolo meccanismo, ma di una combinazione di fattori che varia da persona a persona, il che spiega perché non esiste un trattamento unico che funzioni per tutti.
La comunità scientifica internazionale ha recentemente sostituito il termine "disturbo funzionale" con "disturbo dell'interazione cervello-intestino", proprio per sottolineare che si tratta di una condizione con basi biologiche reali, anche se non sempre documentabili con gli esami tradizionali.
L'asse cervello-intestino: perché è così importante
Il concetto di asse cervello-intestino è fondamentale per capire la SII. Il cervello e l'intestino comunicano continuamente attraverso una rete complessa di nervi, ormoni e molecole prodotte dai batteri intestinali. Questa comunicazione è bidirezionale: il cervello influenza l'intestino, ma l'intestino influenza anche il cervello. (Figura 1)
Questo spiega perché lo stress e l'ansia possono scatenare sintomi intestinali, ma anche perché problemi intestinali persistenti possono causare ansia e depressione. Un dato importante emerso dalla ricerca è che in circa la metà dei pazienti con SII i sintomi intestinali compaiono prima di quelli psicologici, non dopo. Questo significa che la SII non è semplicemente una conseguenza dello stress, ma che il problema può originare nell'intestino stesso e poi influenzare il cervello.
Circa il 60% dei pazienti con SII presenta un'aumentata sensibilità dell'intestino agli stimoli normali: la distensione causata dal cibo o dai gas, che in una persona sana non causerebbe alcun disagio, viene percepita come dolorosa. Questa condizione, chiamata ipersensibilità viscerale, è uno dei meccanismi centrali della SII e spiega perché i sintomi possono essere così sproporzionati rispetto a ciò che si osserva con gli esami.
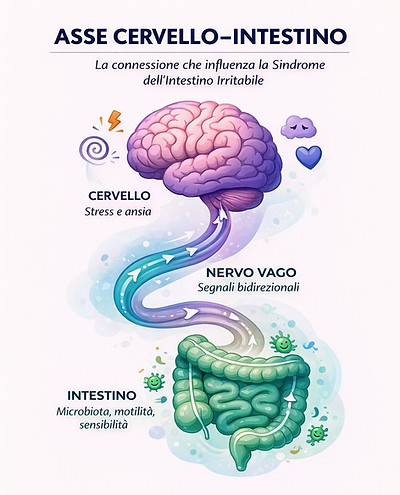
Figura 1: infografica dell’asse cervello-intestino che mostra la comunicazione bidirezionale tra cervello e intestino attraverso il nervo vago.
Stress, emozioni e ansia influenzano la funzione intestinale, mentre microbiota, motilità e sensibilità intestinale possono a loro volta modulare il sistema nervoso, contribuendo ai sintomi della sindrome dell’intestino irritabile.
Quanto è frequente
Le stime di prevalenza della SII variano a seconda dei criteri diagnostici utilizzati e delle aree geografiche studiate. Con i criteri più recenti (Roma IV, più restrittivi dei precedenti), la prevalenza è stimata intorno al 4-5% negli Stati Uniti, nel Regno Unito e in Canada. Con i criteri precedenti (Roma III), le stime erano più alte, intorno al 10-12%.
La SII è più frequente nelle donne e nei soggetti al di sotto dei 50 anni, anche se può manifestarsi a qualsiasi età. La differenza di prevalenza tra i sessi si sta progressivamente riducendo, probabilmente anche per una maggiore consapevolezza e diagnosi nei maschi.
L'impatto economico è significativo: solo negli Stati Uniti, i costi diretti attribuiti alla SII (esclusi i farmaci) sono stimati tra 1,5 e 10 miliardi di dollari all'anno, a cui si aggiungono i costi indiretti legati all'assenteismo lavorativo e alla ridotta produttività.
Forme cliniche
La SII si manifesta in forme diverse, classificate in base al tipo di alterazione dell'abitudine intestinale prevalente. La classificazione si basa sulla Scala di Bristol, uno strumento visivo che descrive sette tipi di feci, dal tipo 1 (feci dure, a palline separate) al tipo 7 (feci completamente liquide). (Figura 2)
-
SII con stipsi (SII-C): feci dure o a palline (Bristol tipo 1-2) in più del 25% delle evacuazioni, e feci molli o liquide in meno del 25%.
-
SII con diarrea (SII-D): feci molli o liquide (Bristol tipo 6-7) in più del 25% delle evacuazioni, e feci dure in meno del 25%.
-
SII mista (SII-M): alternanza di entrambi i pattern, con feci dure in più del 25% e feci molli in più del 25% delle evacuazioni.
-
SII non classificabile (SII-U): quando le alterazioni delle feci non sono sufficienti per rientrare in nessuna delle categorie precedenti.
È importante sapere che i sintomi spesso si sovrappongono tra i sottotipi e che il pattern delle feci può variare anche nell'arco di poche settimane. Molti pazienti passano da un sottotipo all'altro nel corso del tempo.

Figura 2: infografica della Scala di Bristol che classifica le feci in 7 tipi: tipi 1-2 stipsi (palline dure e salsiccia grumosa), tipi 3-4 normali (salsiccia con crepe e liscia e morbida), tipi 5-6 feci molli (pezzetti morbidi e frammenti pastosi), tipo 7 diarrea (liquide). Include consigli: tipi 1-2 più acqua, fibre e movimento; tipi 3-4 continua così; tipi 5-7 attenzione a dieta e stress.: Iinfografica della Scala di Bristol che classifica le feci in 7 tipi: tipi 1-2 stipsi (palline dure e salsiccia grumosa), tipi 3-4 normali (salsiccia con crepe e liscia e morbida), tipi 5-6 feci molli (pezzetti morbidi e frammenti pastosi), tipo 7 diarrea (liquide). Include consigli: tipi 1-2 più acqua, fibre e movimento; tipi 3-4 continua così; tipi 5-7 attenzione a dieta e stress.
Sintomi
I sintomi della SII possono variare considerevolmente da persona a persona, ma quelli che definiscono la sindrome secondo i criteri internazionali sono:
-
Dolore addominale ricorrente: è il sintomo cardine. Può essere crampiforme, sordo o di tipo colico. Caratteristicamente, è collegato alla defecazione (può migliorare o peggiorare con l'evacuazione) e si associa a variazioni della frequenza o della consistenza delle feci.
-
Gonfiore addominale: la sensazione di pancia gonfia e tesa è uno dei sintomi più frequenti e fastidiosi, anche se non è necessario per la diagnosi. Può peggiorare nel corso della giornata e dopo i pasti.
-
Alterazioni dell'abitudine intestinale: diarrea, stipsi o alternanza delle due, come descritto nella sezione sulle forme cliniche.
-
Urgenza defecatoria: il bisogno improvviso e impellente di evacuare, che può essere molto limitante nella vita sociale e lavorativa.
-
Sensazione di evacuazione incompleta: può portare a tentativi ripetuti e poco fruttuosi di evacuazione, che a loro volta favoriscono l'insorgenza di patologia emorroidaria, ragadi e prolassi.
-
Muco nelle feci: la presenza di muco biancastro o semitrasparente è frequente e non deve allarmare, ma va segnalata al medico.
Oltre ai sintomi intestinali, molti pazienti con SII riferiscono anche sintomi extraintestinali: stanchezza cronica, dolori muscolari, cefalea, disturbi urinari e disturbi del sonno. La presenza di questi sintomi non è casuale, ma riflette la natura sistemica del disturbo dell'interazione cervello-intestino.
Cosa scatena o fa peggiorare i sintomi
Diversi fattori possono scatenare o peggiorare i sintomi della SII. Conoscerli è il primo passo per imparare a gestirli.
-
Stress e fattori psicologici. Lo stress emotivo, l'ansia e la depressione sono tra i fattori più potenti nel modulare i sintomi della SII. Non si tratta di "avere i sintomi perché si è stressati", ma di un'interazione biologica reale: lo stress attiva l'asse cervello-intestino, aumenta la sensibilità viscerale e altera la motilità intestinale. I fattori psicosociali sono presenti in una percentuale significativa di pazienti e non vanno trascurati se si vuole affrontare la SII in modo efficace. È spesso difficile stabilire se siano causa o conseguenza della condizione: nella pratica clinica, sono entrambe le cose.
-
Alimentazione. Molti pazienti imparano presto ad associare l'insorgenza dei sintomi con determinati cibi o comportamenti alimentari. I pasti abbondanti, i cibi ricchi di grassi, i cibi piccanti, le bevande gassate, l'alcol e la caffeina sono tra i fattori scatenanti più comuni. Meno frequentemente si fa caso a comportamenti alimentari all'apparenza innocui ma che, protratti nel tempo, diventano fattori che causano e fanno perdurare la SII: saltare i pasti, mangiare troppo velocemente, masticare poco. Questi comportamenti sono costantemente presenti in buona parte delle malattie gastrointestinali e proctologiche.
-
Infezioni gastrointestinali pregresse. Nel 10-20% dei pazienti che hanno avuto una gastroenterite acuta (batterica, virale o protozoaria), i sintomi di tipo SII persistono anche dopo la risoluzione dell'infezione. Questa forma, chiamata SII post-infettiva, è particolarmente frequente e viene spesso scambiata per una recidiva o persistenza della malattia infettiva, portando a trattamenti antibiotici inutili. Il meccanismo sembra coinvolgere un'infiammazione residua della mucosa intestinale e alterazioni del microbiota.
-
Farmaci. Alcuni farmaci possono scatenare o peggiorare i sintomi della SII: antibiotici (che alterano il microbiota), antinfiammatori non steroidei (FANS), e alcuni antidepressivi. È importante segnalare sempre al medico tutti i farmaci che si assumono.
-
Ciclo mestruale. Le fluttuazioni ormonali del ciclo mestruale possono influenzare la sensibilità rettale e la motilità intestinale, causando variazioni dei sintomi in fase premestruale e mestruale.
-
Viaggi. I cambiamenti dei ritmi di vita, degli orari dei pasti, della qualità dell'acqua e dell'alimentazione possono scatenare la SII nei soggetti predisposti.
Il ruolo del Microbiota intestinale
Il microbiota intestinale — l'insieme dei miliardi di microrganismi che abitano il nostro intestino — è uno degli argomenti più studiati e discussi in relazione alla SII. È anche uno dei temi su cui circolano più informazioni fuorvianti, spesso veicolate da chi vende integratori.
Cosa sappiamo con ragionevole certezza: studi hanno dimostrato che il microbiota dei pazienti con SII è spesso diverso da quello delle persone sane, con una ridotta diversità microbica e alterazioni nella composizione delle specie batteriche. Queste alterazioni possono influenzare la fermentazione intestinale (producendo più gas), la permeabilità della mucosa e la comunicazione con il sistema nervoso.
Cosa non sappiamo ancora: non è chiaro se le alterazioni del microbiota siano una causa della SII o una sua conseguenza. Non esiste un "profilo microbico" specifico della SII e non siamo ancora in grado di correggere in modo mirato queste alterazioni nella pratica clinica quotidiana.
Questo argomento è in rapida evoluzione e verrà approfondito in due pagine dedicate: una che prende spunto dal meteorismo intestinale e una che spiega il microbiota in modo accessibile anche ai più giovani.
La Diagnosi
La diagnosi di SII è clinica: si basa cioè sui sintomi riferiti dal paziente e non richiede necessariamente esami invasivi. I criteri diagnostici attualmente utilizzati a livello internazionale sono i criteri di Roma IV (2016), che definiscono la SII come:
Dolore addominale ricorrente, presente in media almeno un giorno alla settimana negli ultimi tre mesi, associato ad almeno due delle seguenti condizioni:
-
il dolore è collegato alla defecazione (migliora o peggiora);
-
il dolore si associa a una variazione della frequenza delle evacuazioni;
-
il dolore si associa a un cambiamento della consistenza delle feci.
-
I sintomi devono essere presenti da almeno sei mesi.
Un aspetto importante: la diagnosi di SII è una diagnosi "positiva", basata sulla presenza di sintomi caratteristici, e non semplicemente una diagnosi di esclusione.
Tuttavia, il medico dovrà escludere altre condizioni che possono presentarsi con sintomi simili, come la celiachia, le malattie infiammatorie intestinali e, nei soggetti a rischio, il cancro del colon-retto.
Gli esami di base raccomandati dalle linee guida includono: emocromo completo, proteina C reattiva (PCR) e anticorpi anti-transglutaminasi (per escludere la celiachia). In caso di diarrea predominante, può essere utile dosare la calprotectina fecale per escludere una malattia infiammatoria intestinale.
Quando sono necessari esami più approfonditi
Esami più approfonditi, come la colonscopia, trovano indicazione quando sono presenti i cosiddetti "segni d'allarme":
-
Età superiore ai 50 anni con sintomi di nuova insorgenza
-
Insorgenza improvvisa dei sintomi
-
Calo di peso non giustificato
-
Presenza di sangue nelle feci o anemia da carenza di ferro (sideropenica)
-
Familiarità per cancro del colon-retto o malattie infiammatorie intestinali
-
Diarrea notturna (che sveglia dal sonno)
-
Febbre inspiegata
-
Massa addominale palpabile
In assenza di segni d'allarme, in un paziente giovane con sintomi tipici, la diagnosi può essere posta con ragionevole sicurezza sulla base dei criteri clinici, senza necessità di esami invasivi. Questo approccio è raccomandato dalle principali linee guida internazionali (ACG, NICE, BSG) e riduce i costi, i tempi e l'ansia legata a esami non necessari.
Alimentazione e sindrome dell'intestino irritabile
La dieta influenza in modo importante i sintomi della SII. La maggior parte dei pazienti lo sa per esperienza diretta. Le linee guida NICE raccomandano come primo passo una serie di consigli alimentari e di stile di vita generali, prima di passare a diete più restrittive.
-
Consumare pasti regolari, senza saltarli, e prendersi il tempo per mangiare con calma.
-
Bere almeno 8 bicchieri di liquidi non contenenti caffeina al giorno.
-
Limitare la caffeina a non più di 3 tazze al giorno.
-
Evitare o ridurre alcol e bevande gassate.
-
Limitare la frutta fresca a non più di 3 porzioni al giorno.
-
Ridurre gli amidi resistenti (patate, pasta e riso riscaldati dopo la cottura).
-
Evitare i dolcificanti artificiali contenenti sorbitolo o mannitolo.
-
Fare attività fisica regolare: anche una camminata quotidiana può migliorare significativamente i sintomi.
Questi consigli, apparentemente semplici, producono un miglioramento dei sintomi nel 42-44% dei pazienti. Non sono da sottovalutare.
Per quanto riguarda le fibre, la situazione è più sfumata di quanto si pensi comunemente. Le fibre solubili (come lo psillio, noto anche come ispagula) hanno dimostrato un beneficio modesto ma significativo. Le fibre insolubili (come la crusca di frumento) non hanno dimostrato benefici e possono addirittura peggiorare il gonfiore e il dolore in alcuni pazienti. Se si decide di aumentare l'apporto di fibre, è fondamentale farlo gradualmente per evitare un peggioramento dei sintomi.
La dieta a basso contenuto di FODMAP
Con l'acronimo FODMAP si indica un gruppo di carboidrati a catena corta (Fermentable Oligosaccharides, Disaccharides, Monosaccharides And Polyols) che vengono scarsamente assorbiti nell'intestino tenue. Quando raggiungono il colon, vengono fermentati dai batteri intestinali producendo gas, e richiamano acqua nel lume intestinale per effetto osmotico. Nella maggior parte delle persone questo processo è del tutto normale e benefico. In alcuni individui, però, può scatenare dolore, gonfiore e alterazioni dell'abitudine intestinale. (Figura 3)
Le linee guida NICE raccomandano la dieta a basso contenuto di FODMAP come seconda linea di intervento dietetico, quando i consigli alimentari generali non sono sufficienti. L'American College of Gastroenterology (ACG) la raccomanda con un livello di evidenza condizionale. Una meta-analisi del 2022 pubblicata su Gut l'ha identificata come l'intervento dietetico più efficace per migliorare i sintomi globali della SII.
Tuttavia, è importante conoscere anche i limiti di questa dieta. Le revisioni sistematiche hanno evidenziato che gli studi disponibili sono di breve durata (mai superiore a 6 settimane), hanno un alto rischio di bias e non hanno valutato adeguatamente la fase di reintroduzione degli alimenti. Alcuni esperti ritengono che parte del beneficio osservato possa essere attribuito all'effetto placebo. Inoltre, una restrizione prolungata dei FODMAP può causare alterazioni sfavorevoli del microbiota intestinale e carenze nutrizionali.
La dieta FODMAP non è una dieta permanente. Si articola in tre fasi: una fase di eliminazione (2-6 settimane), una fase di reintroduzione graduale dei singoli gruppi di FODMAP per identificare quelli che causano problemi, e una fase di personalizzazione a lungo termine. Deve essere seguita sotto la guida di un nutrizionista esperto. Il fai-da-te espone al rischio di un'alimentazione squilibrata e controproducente.
Tra gli alimenti ad alto contenuto di FODMAP ci sono: frumento, orzo, segale e loro derivati; legumi come fagioli, ceci e lenticchie; alcuni frutti come mele, pere, anguria, albicocche; verdure come cipolla, aglio, carciofi, cavolfiore, asparagi; latte vaccino e latticini freschi; frutta secca come anacardi e pistacchi; dolcificanti artificiali.
Tra gli alimenti a basso contenuto di FODMAP: riso, avena, quinoa; banane, mirtilli, uva, mandarini, fragole; pomodori, carote, cetrioli, spinaci, peperoni, zucchine; sostituti vegetali del latte (mandorla, riso, soia senza additivi); patate; formaggi stagionati.
Un recente studio svedese (CARIBS, 2024) ha confrontato direttamente la dieta FODMAP con il trattamento farmacologico ottimizzato, dimostrando che entrambi gli approcci producono miglioramenti significativi dei sintomi. Questo conferma che la dieta è un'opzione terapeutica valida, ma non necessariamente superiore ai farmaci.

Figura 3: infografica completa sulla dieta FODMAP nella sindrome dell’intestino irritabile (IBS o colon irritabile), utile per riconoscere rapidamente gli alimenti da limitare e quelli generalmente meglio tollerati. I FODMAP sono carboidrati fermentabili che possono causare gonfiore addominale, dolore, meteorismo e alterazioni dell’alvo (diarrea o stipsi) nei soggetti sensibili.
Nell’infografica sono riportati esempi pratici della dieta italiana quotidiana — come pane, pasta, pizza, latticini, frutta, verdura, legumi e bevande — per facilitare scelte alimentari più consapevoli. Gli alimenti ad alto contenuto di FODMAP (come alcuni cereali, latticini con lattosio, legumi e specifici tipi di frutta e verdura) sono associati più frequentemente ai sintomi, mentre le alternative a basso contenuto di FODMAP possono contribuire a migliorare il benessere intestinale.
È importante ricordare che la risposta ai FODMAP è altamente individuale: la dieta dovrebbe essere personalizzata, preferibilmente con il supporto di uno specialista, attraverso una fase di riduzione seguita da una graduale reintroduzione degli alimenti. Questa guida ha scopo informativo e non sostituisce una valutazione medica o nutrizionale.
Terapia farmacologica
Il trattamento farmacologico della SII è personalizzato in base al sintomo predominante. L'approccio è graduale: si inizia con i farmaci di prima linea, più semplici e accessibili, e si intensifica solo se necessario.
Trattamenti di prima linea (disponibili in Italia)
Per il dolore addominale crampiforme: gli antispasmodici (come la scopolamina butilbromuro, la mebeverina, l'otilonio bromuro e il pinaverio bromuro) sono il trattamento di prima scelta. L'olio di menta piperita in capsule gastroresistenti ha dimostrato un'efficacia moderata ed è ben tollerato.
Per la stipsi: i lassativi osmotici (come il macrogol/polietilenglicole) migliorano la frequenza delle evacuazioni, anche se non hanno dimostrato un effetto significativo sul dolore. Le fibre solubili (psillio/ispagula) possono essere utili.
Per la diarrea: la loperamide riduce la frequenza delle evacuazioni e migliora la consistenza delle feci. Non ha un effetto significativo sul dolore, ma è utile per gestire l'urgenza e la diarrea.
Trattamenti di seconda linea: i neuromodulatori
Quando i trattamenti di prima linea non sono sufficienti, le linee guida internazionali raccomandano l'uso di neuromodulatori centrali, in particolare gli antidepressivi triciclici (TCA) a basso dosaggio. È fondamentale chiarire un punto: questi farmaci non vengono prescritti perché la SII è un disturbo psicologico, ma perché agiscono sui meccanismi di comunicazione tra cervello e intestino, riducendo la sensibilità viscerale e modulando la motilità.
Il trial ATLANTIS (2023), il più grande studio mai condotto su un antidepressivo triciclico nella SII, ha dimostrato che l'amitriptilina a basso dosaggio (10-30 mg alla sera) è superiore al placebo come trattamento di seconda linea nelle cure primarie, con un buon profilo di sicurezza e tollerabilità. Gli effetti collaterali più comuni (sonnolenza e bocca secca) sono generalmente lievi. L'effetto terapeutico non dipende dall'azione antidepressiva: i dosaggi utilizzati sono molto inferiori a quelli necessari per trattare la depressione.
I TCA sono particolarmente indicati per i pazienti con dolore predominante e/o diarrea, perché rallentano il transito intestinale. Per i pazienti con stipsi predominante, possono essere preferibili gli inibitori selettivi della ricaptazione della serotonina (SSRI) o le amine secondarie (come la nortriptilina), che hanno minori effetti costipanti.
Farmaci specifici approvati dalla FDA (disponibilità in Italia variabile)
Per la SII con stipsi (SII-C): linaclotide (disponibile in Italia, è il farmaco con il livello di evidenza più alto secondo le linee guida AGA), lubiprostone, plecanatide e tenapanor. Questi farmaci agiscono sui canali ionici delle cellule intestinali, aumentando la secrezione di acqua nel lume e accelerando il transito. La diarrea è l'effetto collaterale più comune. Lubiprostone, plecanatide e tenapanor non sono attualmente commercializzati in Italia.
Per la SII con diarrea (SII-D): rifaximina (disponibile in Italia, antibiotico non assorbibile, somministrato in cicli di 14 giorni, ripetibili), eluxadolina e alosetron. Eluxadolina è controindicata nei pazienti senza colecisti per il rischio di pancreatite. Alosetron è stato a lungo soggetto a restrizioni per il rischio di colite ischemica. Eluxadolina e alosetron non sono disponibili in Italia.
Ondansetron (disponibile in Italia, utilizzato off-label): un antagonista dei recettori 5-HT3 con un eccellente profilo di sicurezza, che migliora l'urgenza e la frequenza delle evacuazioni nella SII-D.
Nota importante: gli oppioidi centrali (come tramadolo, codeina, ossicodone) non sono raccomandati per il dolore della SII. Non solo non hanno dimostrato efficacia, ma possono peggiorare la condizione a lungo termine attraverso il meccanismo dell'iperalgesia indotta da oppioidi e la dipendenza.
Le terapie psicologiche e comportamentali
Le terapie psicologiche non sono un'alternativa ai farmaci, ma un complemento fondamentale, soprattutto nei pazienti con sintomi moderati-severi o con una significativa componente di ansia e ipervigilanza.
La terapia cognitivo-comportamentale (CBT) focalizzata sull'apparato gastrointestinale e l'ipnoterapia diretta all'intestino (gut-directed hypnotherapy) sono gli interventi con le migliori evidenze di efficacia. Agiscono modificando i circuiti di comunicazione tra cervello e intestino, riducendo l'amplificazione centrale dei segnali dolorosi provenienti dall'intestino.
Tecniche di gestione dello stress come la mindfulness, lo yoga e le tecniche di rilassamento possono essere utili come complemento, anche se le evidenze scientifiche sono meno robuste.
Un modello di cura integrato, in cui interventi comportamentali, modifiche dietetiche e farmaci vengono considerati come partner alla pari, offre le migliori probabilità di successo.
Sindrome dell'intestino irritabile e malattie proctologiche
Questo è un aspetto che merita particolare attenzione e che viene spesso sottovalutato. La SII può avere un impatto considerevole su molte condizioni coloproctologiche, influenzandone l'insorgenza, l'evoluzione e la risposta ai trattamenti.
La prevalenza di disfunzioni del pavimento pelvico nei pazienti con SII è stimata fino al 40%. Molti pazienti con SII-C presentano una defecazione dissinergica (una mancata coordinazione dei muscoli del pavimento pelvico durante l'evacuazione) che contribuisce alla sensazione di evacuazione incompleta, allo sforzo eccessivo e, di conseguenza, all'insorgenza di emorroidi, ragadi e prolassi.
I tentativi ripetuti di evacuazione, tipici della SII, sottopongono le strutture anorettali a uno stress meccanico cronico. Questo può ritardare la guarigione dopo interventi proctologici o favorire le recidive, che sarebbe forse più corretto definire "incomplete guarigioni".
Nella SII-D, l'urgenza defecatoria e la diarrea cronica possono contribuire all'insorgenza di incontinenza fecale e di irritazione perianale.
Per questo motivo, in un paziente con patologia coloproctologica che non risponde adeguatamente ai trattamenti o che presenta recidive frequenti, è importante valutare la coesistenza di una SII e trattarla in modo appropriato. Ignorare questa componente significa spesso condannarsi a risultati terapeutici insoddisfacenti.

Come prenotare una visita proctologica a Roma
con il Dott. Daffinà
Prenota online, in pochi secondi e senza attese telefoniche utilizzando il pusante
(Apre miodottore in una nuova scheda)
Oppure, visita questa pagina per avere tutte le informazioni
Probiotici: cosa dice davvero la scienza
I probiotici sono tra i prodotti più pubblicizzati per la SII, con un mercato che muove miliardi di euro. È quindi particolarmente importante distinguere ciò che è dimostrato da ciò che è marketing.
La meta-analisi più recente e completa (Goodoory et al., Gastroenterology 2023, 82 studi, oltre 10.000 pazienti) ha concluso che alcuni ceppi o combinazioni di probiotici possono essere utili nella SII, ma che il livello di certezza delle evidenze è basso o molto basso per quasi tutte le analisi. Solo 24 dei 82 studi inclusi avevano un basso rischio di bias.
Le linee guida ACG suggeriscono i probiotici come gruppo per migliorare i sintomi globali, il gonfiore e la flatulenza, ma con una raccomandazione debole e un livello di evidenza basso. L'AGA (American Gastroenterological Association) non è in grado di raccomandare ceppi specifici per la SII, dato che la maggior parte dei probiotici è stata testata in un solo studio.
Cosa sappiamo con ragionevole certezza: una revisione sistematica strain-specifica del 2026 ha identificato alcuni ceppi con evidenza di efficacia in meta-analisi: Bifidobacterium longum 35624 (precedentemente chiamato Bifidobacterium infantis), Lactobacillus rhamnosus GG, Lactiplantibacillus plantarum 299v, Saccharomyces cerevisiae CNCM I-3856 e Bacillus coagulans Unique IS2. Per altri ceppi, i risultati sono contrastanti o insufficienti.
Dose e durata: le evidenze suggeriscono che una dose minima di 10 miliardi di unità formanti colonie al giorno possa essere necessaria per ottenere un beneficio, e che l'effetto terapeutico possa manifestarsi dopo almeno 4 settimane di trattamento. Tuttavia, la durata ottimale del trattamento non è stata stabilita.
Il problema principale: esistono centinaia di ceppi diversi, e ciò che funziona per un ceppo non può essere generalizzato ad altri. Quando si acquista un probiotico, è fondamentale verificare che il ceppo specifico (non solo il genere e la specie, ma anche il codice identificativo del ceppo) sia stato testato in studi clinici nella SII. La maggior parte dei prodotti in commercio non soddisfa questo criterio.
Sicurezza: i probiotici sono generalmente sicuri. In 55 studi che hanno incluso oltre 7.000 pazienti, il rischio di eventi avversi non è risultato significativamente più alto con i probiotici rispetto al placebo.
L'esperienza clinica quotidiana suggerisce che alcuni pazienti traggono beneficio dai probiotici, ma è impossibile prevedere chi risponderà. Se si decide di provare un probiotico, è ragionevole scegliere un ceppo con evidenze documentate, assumerlo per almeno 4-8 settimane a dose adeguata, e valutare criticamente se si ottiene un beneficio reale. Se non si osserva alcun miglioramento dopo questo periodo, è inutile continuare.
Il loro impiego prolungato ha un costo economico importante che va considerato. Si può ovviare parzialmente ricorrendo al consumo regolare di alimenti naturalmente ricchi di probiotici, come yogurt con fermenti vivi, kefir e alimenti fermentati, anche se le concentrazioni di batteri vivi sono generalmente inferiori rispetto agli integratori.
Cosa aspettarsi nel tempo
La SII è una condizione cronica, ma questo non significa che i sintomi saranno sempre presenti con la stessa intensità. Il decorso tipico della SII è caratterizzato da fluttuazioni: periodi di sintomi più intensi si alternano a periodi di relativo benessere o addirittura di completa remissione.
Studi longitudinali hanno dimostrato che l'incidenza di nuovi casi di SII è di circa 1,5-2,5% all'anno, ma la prevalenza nella popolazione rimane stabile nel tempo. Questo perché il numero di persone che sviluppano nuovi sintomi è bilanciato dal numero di persone i cui sintomi scompaiono o si attenuano. In studi di popolazione, la proporzione di pazienti che riferisce una risoluzione dei sintomi varia dal 17% al 55%, a seconda dei criteri utilizzati e della durata del follow-up.
Anche i sottotipi di SII non sono stabili nel tempo. In uno studio su pazienti seguiti per 12 mesi, solo uno su quattro ha mantenuto la stessa classificazione per tutto il periodo. Due pazienti su tre con SII-C o SII-D sono passati alla forma mista (SII-M), che risulta essere il sottotipo meno stabile. Questo significa che un paziente che oggi ha prevalentemente diarrea potrebbe, tra qualche mese, avere prevalentemente stipsi, o alternare le due condizioni.
Fattori associati a una maggiore gravità e persistenza dei sintomi includono: la sovrapposizione con altri disturbi gastrointestinali funzionali (come la dispepsia funzionale), la presenza di ansia e depressione significative, una storia di abuso fisico o sessuale, e un elevato numero di visite mediche e di esami diagnostici (che riflette spesso un'ansia di malattia non risolta).
Un dato importante: la SII causa morbilità (riduzione della qualità di vita), ma non mortalità. Non aumenta il rischio di sviluppare malattie infiammatorie intestinali o cancro del colon-retto. Questo è un messaggio rassicurante che va sottolineato, perché molti pazienti vivono con la paura che i loro sintomi siano il segnale di qualcosa di più grave.
Nessuna terapia medica ha dimostrato di modificare la storia naturale della SII a lungo termine. La maggior parte degli studi clinici ha una durata di 12 settimane, e non sappiamo se i benefici osservati si mantengono nel tempo. Questo non significa che il trattamento sia inutile, ma che l'obiettivo realistico è il controllo dei sintomi, non la guarigione definitiva.
Con il giusto approccio — che include modifiche dello stile di vita, gestione dello stress, interventi dietetici mirati e, quando necessario, farmaci — la grande maggioranza dei pazienti può ottenere un miglioramento significativo della qualità di vita e vivere in modo pieno e attivo.
Domande frequenti
La SII è una malattia psicologica?
No. La SII è un disturbo dell'interazione cervello-intestino con basi biologiche documentate. È vero che fattori psicologici come stress, ansia e depressione possono influenzare i sintomi, ma questo non significa che la SII sia "tutta nella testa". Il cervello e l'intestino comunicano continuamente, e alterazioni in questa comunicazione possono causare sintomi reali e invalidanti. In circa la metà dei pazienti, i sintomi intestinali compaiono prima di quelli psicologici, non dopo.
La SII può trasformarsi in qualcosa di più grave?
No. La SII non aumenta il rischio di sviluppare malattie infiammatorie intestinali (come il morbo di Crohn o la colite ulcerosa) o cancro del colon-retto. È una condizione cronica che causa morbilità ma non mortalità. Tuttavia, se compaiono segni d'allarme (sangue nelle feci, calo di peso inspiegato, febbre, sintomi che svegliano dal sonno), è fondamentale consultare il medico per escludere altre condizioni.
Devo eliminare il glutine dalla mia dieta?
Non necessariamente. La celiachia deve essere esclusa con un esame del sangue (anticorpi anti-transglutaminasi) prima di eliminare il glutine. Se il test è negativo, non c'è indicazione a eliminare completamente il glutine. Tuttavia, alcuni pazienti con SII riferiscono un miglioramento riducendo i cereali contenenti glutine, probabilmente perché questi alimenti sono anche ricchi di FODMAP. Se si decide di provare, è importante farlo sotto la guida di un nutrizionista per evitare carenze nutrizionali.
I probiotici funzionano davvero?
Alcuni ceppi specifici di probiotici hanno dimostrato un beneficio modesto in studi clinici, ma il livello di certezza delle evidenze è basso. Non tutti i probiotici sono uguali: ciò che funziona per un ceppo non può essere generalizzato ad altri. Se si decide di provare un probiotico, è importante scegliere un ceppo con evidenze documentate, assumerlo a dose adeguata (almeno 10 miliardi di unità formanti colonie al giorno) per almeno 4-8 settimane, e valutare criticamente se si ottiene un beneficio reale.
Quanto tempo ci vuole per vedere un miglioramento con la dieta FODMAP?
La fase di eliminazione della dieta FODMAP dura tipicamente 2-6 settimane. Alcuni pazienti riferiscono un miglioramento già dopo 2-3 settimane. È fondamentale ricordare che questa non è una dieta permanente: dopo la fase di eliminazione, si procede con la reintroduzione graduale degli alimenti per identificare quali FODMAP causano problemi. La dieta deve essere seguita sotto la guida di un nutrizionista esperto.
Posso guarire completamente dalla SII?
La SII è una condizione cronica, ma i sintomi fluttuano nel tempo. Studi di popolazione hanno dimostrato che una percentuale significativa di pazienti (17-55% a seconda degli studi) riferisce una risoluzione dei sintomi nel corso degli anni. Con il trattamento appropriato, la grande maggioranza dei pazienti può ottenere un controllo soddisfacente dei sintomi e vivere una vita normale e attiva. L'obiettivo realistico è il controllo dei sintomi, non necessariamente la guarigione definitiva.
La SII può influenzare altre condizioni coloproctologiche?
Sì, e questo è un aspetto spesso sottovalutato. La SII può peggiorare l'evoluzione di emorroidi, ragadi, prolassi e incontinenza fecale, ritardandone la guarigione o favorendo le recidive. I tentativi ripetuti di evacuazione, tipici della SII, sottopongono le strutture anorettali a uno stress meccanico cronico. Per questo motivo, in un paziente con patologia coloproctologica che non risponde adeguatamente ai trattamenti, è importante valutare e trattare una eventuale SII sottostante.
Devo prendere farmaci per tutta la vita?
Non necessariamente. I farmaci vengono utilizzati per controllare i sintomi quando le modifiche dello stile di vita e della dieta non sono sufficienti. Molti pazienti utilizzano i farmaci in modo intermittente, durante i periodi di riacutizzazione dei sintomi, e li sospendono quando stanno meglio. La decisione va presa insieme al medico, in base alla gravità e alla frequenza dei sintomi.
Conclusioni
La Sindrome dell'Intestino Irritabile è una condizione reale, riconosciuta dalla comunità scientifica internazionale, con meccanismi biologici documentati. Non è una malattia immaginaria e non è "solo stress".
È una condizione cronica che può essere molto invalidante, ma è anche una condizione trattabile. La maggior parte dei pazienti può ottenere un miglioramento significativo con un approccio combinato che include modifiche dello stile di vita, interventi dietetici mirati, gestione dello stress e, quando necessario, farmaci appropriati.
Il trattamento richiede tempo, costanza e un rapporto di fiducia con il proprio medico. Non esistono soluzioni rapide, nonostante ciò che si legge sui social media o nelle pubblicità di integratori. Ogni paziente è diverso, e ciò che funziona per uno può non funzionare per un altro. È fondamentale personalizzare il trattamento e avere aspettative realistiche.
Un aspetto spesso trascurato è l'impatto della SII su altre condizioni coloproctologiche. Se soffri di emorroidi, ragadi, prolassi o incontinenza che non rispondono adeguatamente ai trattamenti o che recidivano frequentemente, è importante valutare e trattare una eventuale SII associata.
Con il giusto supporto e un approccio integrato, è possibile convivere con la SII mantenendo una buona qualità di vita e partecipando pienamente alle attività quotidiane, lavorative e sociali.
Bibliografia
-
Ford AC, Lacy BE, Talley NJ. Irritable Bowel Syndrome. N Engl J Med. 2017;377(26):2566-2578.
-
Ford AC, Sperber AD, Corsetti M, Camilleri M. Irritable Bowel Syndrome. Lancet. 2020;396(10263):1675-1688.
-
Wang L, Alammar N, Singh R, et al. Gut Microbial Dysbiosis in the Irritable Bowel Syndrome: A Systematic Review and Meta-Analysis of Case-Control Studies. J Acad Nutr Diet. 2020;120(4):565-586.
-
Aziz I, Simrén M. The Overlap Between Irritable Bowel Syndrome and Organic Gastrointestinal Diseases. Lancet Gastroenterol Hepatol. 2021;6(2):139-148.
-
Camilleri M. Diagnosis and Treatment of Irritable Bowel Syndrome: A Review. JAMA. 2021;325(9):865-877.
-
Lacy BE, Pimentel M, Brenner DM, et al. ACG Clinical Guideline: Management of Irritable Bowel Syndrome. Am J Gastroenterol. 2021;116(1):17-44.
-
Wechsler EV, Shah ED. Diarrhea-Predominant and Constipation-Predominant Irritable Bowel Syndrome: Current Prescription Drug Treatment Options. Drugs. 2021;81(17):1953-1968.
-
Wilkinson JM, Gill MC. Irritable Bowel Syndrome: Questions and Answers for Effective Care. Am Fam Physician. 2021;103(12):727-736.
-
Black CJ, Staudacher HM, Ford AC. Efficacy of a Low FODMAP Diet in Irritable Bowel Syndrome: Systematic Review and Network Meta-Analysis. Gut. 2022;71(6):1117-1126.
-
Khalighi Sikaroudi M, Soltani S, Ghoreishy SM, et al. Effects of a Low FODMAP Diet on the Symptom Management of Patients With Irritable Bowel Syndrome: A Systematic Umbrella Review With the Meta-Analysis of Clinical Trials. Food Funct. 2024;15(13):6817-6832.
-
Hung KW, Leiman DA, Kaza A, et al. AGA Institute Quality Indicator Development for Irritable Bowel Syndrome. Gastroenterology. 2025;168(3):456-467.
-
Li X, Yuan Q, Huang H, Wang L. Gut Microbiota in Irritable Bowel Syndrome: A Narrative Review of Mechanisms and Microbiome-Based Therapies. Front Immunol. 2025;16:1523456.
-
Andoh A, Miwa H. Association Between the Gut Microbiota and the Pathophysiology of Irritable Bowel Syndrome: A Narrative Review. Digestion. 2026;105(2):89-101.
-
Singh P, Lee A, Sheth NM, Chey WD. Chronic, Noninfectious Diarrhea. JAMA. 2026;335(8):678-689.
